Antwort E
zurück zur Frage |
 |
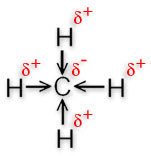
Aufgrund der Elektronegativitätsdifferenz der Bindungspartner ist die CH-Bindung nur leicht polarisiert (ΔEN = 0,3).
Aber auch ein stark polarisiertes Molekül, z.B. CF4, wäre kein Dipol, da die Partialladungen symmetrisch verteilt sind.
Dies folgt aus der Vektoraddition der einzelnen Dipolmomente, welche sich gegenseitig aufheben.
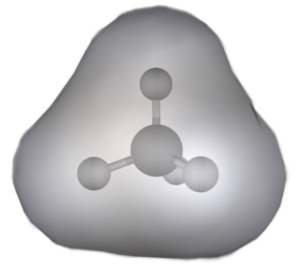
Elektrostatisches Potential von Methan Farbskala von blau (elektronenarm) bis rot (elektronenreich)
(Für eine Animation ins Bild klicken)