Eisenaufnahme
Obwohl Eisen das vierthäufigste chemische Element in der Erdkruste ist, ist seine Bioverfügbarkeit relativ gering. In der Sauerstoffatmosphäre der Erde liegt praktisch alles Eisen in der Oxidationsstufe +3 vor. Das Löslichkeitsprodukt für Fe(OH)3 ist mit 2 • 1039 mol4 • l-4 außerordentlich gering, sodass insbesondere bei Böden mit höheren pH-Werten (z.B. in Regionen, in denen das Gestein bevorzugt aus Kalkstein oder Dolomit besteht) sehr schnell Eisenmangel auftreten kann. Die Aufnahme in Pflanzenwurzeln erfolgt meist in Form von Fe2+, durch "komplexchemische Mobilisierung" wird das praktisch unlösliche Fe3+ verfügbar. Insbesondere Mikroorganismen besitzen dabei die Fähigkeit, besondere Liganden für Fe3+ herzustellen.
Solche Liganden nennt man Siderophore und sie bilden oktaedrische Fe3+-Komplex mit ausgesprochen hoher (thermodynamischer) Stabilität. Die Remobilisierung erfolgt entweder unter Ausnutzung der (kinetischen) Labilität solcher Verbindungen und/oder durch Redoxprozesse, da die meisten Siderophore ausschließlich Fe3+ binden.
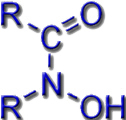
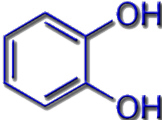
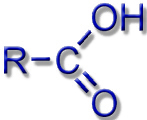
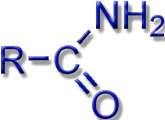
Die meisten bekannten Siderophore greifen auf die gleichen chemischen Grundmuster (Ligandsysteme) zurück: Hydroxamate, Catecholate oder Proteinbausteine.
Hydroxamate |
Catecholate |
Carboxylate, Amine, Amide |
|
|
|
|