Massenwirkungsgesetz
Das Massenwirkungsgesetz beschreibt das Verhältnis der Aktivitäten (oder vereinfacht der Konzentrationen) der an einer chemischen Reaktion beteiligten Stoffe im Gleichgewichtszustand. Dieses Verhältnis ist im Gleichgewichtszustand konstant.
Den Zustand des chemischen Gleichgewichts kann man sich als eine Situation vorstellen bei der die Geschwindigkeiten der Hin- und Rückreaktionen jeweils gleich sind, ohne dass die chemische Reaktion damit "zum Stillstand" gekommen ist.
Das Massenwirkungsgesetz gilt für alle reversiblen Reaktionen, die im Gleichgewicht vorliegen. Die abgeleitete Gleichgewichtskonstante K besitzt einen für die betrachtete Reaktion festen Wert, der jedoch über äußere Einflüsse wie die Temperatur oder (bei Gasreaktionen) den Druck beeinflusst werden kann.
Mit der Möglichkeit zur Einflussnahme auf die Lage eines chemischen Gleichgewichtes und der Berechnung der Konzentration eines Reaktionspartners (z.B. eines Reaktionsproduktes) aus denen der anderen kommt dem Massenwirkungsgesetz eine grundsätzliche Bedeutung bei der quantitativen Betrachtung chemischer Reaktionen und bei der Optimierung von Ausbeuten in industriellen Prozessen zu.
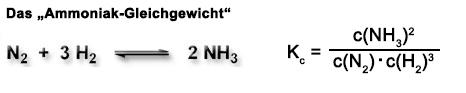
Die Fragen zu diesem Komplex betrachten die Größen des Massenwirkungsgesetzes für reale und fiktive chemische Gleichgewichtsreaktionen und die Möglichkeiten, Einfluss auf diese Größen zu nehmen.
