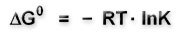Frage 5 - Antwort B
zurück zur Frage |
 |

Für die exergone Reaktion (2) liegt das chemische Gleichgewicht deutlich auf der Seite der Produkte (K > 1).
Für Teilreaktion (1) liegt es auf der Seite der Edukte.
Allgemein gilt:
|
|
ΔG0 = Änderung der freien Enthalpie (Standardbedingungen) R = Gaskonstante T = Temperatur K = Gleichgewichtskonstante |