Frage 7 - Antwort C
zurück zur Frage |
 |
Bei einer Ammoniak-Lösung handelt es sich um eine schwache Base.
Der pOH-Wert schwacher Basen berechnet sich gemäß:
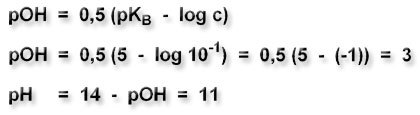
NaOH ist eine starke Base und damit vollständig dissoziiert.
Damit gilt:
Eine 0,1 molare NaOH-Lösung hat eine OH--Ionenkonzentration von 0,1 mol/l (entspricht 10-1).
Das heißt, dass der pOH-Wert = 1 und damit der pH-Wert der Lösung gleich 13 ist.
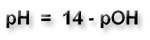
Damit ist der pH-Wert von (1) kleiner als der von (2).
