Frage 6 - Antwort D
zurück zur Frage |
 |
Der Äquivalenzpunkt einer Titration repräsentiert den Wendepunkt der jeweiligen Titrationskurve.
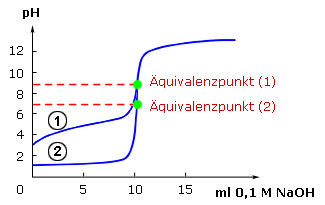
Titration einer schwachen (1) und einer starken
|
Sein pH-Wert ergibt sich aus den Eigenschaften der Bei Titration einer (a) starken Säure mit einer starken Base nahe pH 7 (b) starken Base mit einer starken Säure nahe pH 7 (c) schwachen Säure mit einer starken Base pH > 7 (d) starken Säure mit einer schwachen Base pH < 7 Im Beispiel repräsentiert Kurve (1) die Titration einer schwachen Säure mit einer starken Base und Kurve (2) die Titration einer starken Säure mit einer starken Base. Die Äquivalenzpunkte der beiden Titrationen können also nicht übereinstimmen. |
