Frage 3 - Antwort A
zurück zur Frage |
 |
Phosphorsäure, H3PO4 ist eine dreiprotonige Säure. Sie gibt ihre Protonen in drei Dissoziationsstufen ab:

Die beiden mittleren Dissoziationstufen [H2PO4-] und [HPO42-] sind Ampholyte, das heißt, sie können jeweils als Säure oder Base fungieren.
Damit sind Mischungen dieser Salze Puffersysteme, in denen [H2PO4-] die Säure ist und [HPO42-] als Base (Salz) wirkt.
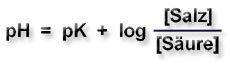
Henderson-Hasselbalch-Gleichung |
Der pH-Wert eines Puffers bestimmt sich nach der Henderson-Hasselbalch-Gleichung. Für den pH-Wert des Puffers ist demnach nur der Quotient der Konzentrationen von Säure und Base entscheidend, nicht der absolute Wert der Konzentration. Im Beispiel sind die Konzentrationen von [H2PO4-] und [HPO42-] jeweils gleich. Das heißt, der Quotient [Salz]/[Säure] wird jeweils 1. Damit haben beide Puffer den gleichen pH-Wert, der dem pK-Wert entspricht. |
