Frage 5 - Antwort B
zurück zur Frage |
 |
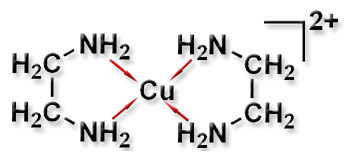
Das Zentralion Cu2+ ist über vier Bindungen an die beiden Chelatliganden Ethylendiamin gebunden.
Die Koordinationszahl des Metalls ist deshalb "4".
Typische Koordinationsumgebungen für Zentralionen mit der Koordinationszahl 4 sind tetraedrisch oder quadratisch-planar.
|
|
|
[Cu(Ethylendiamin)2]2+-Komplex |
Koordinationsumgebung des Kupfers(für die Bilddarstellung hier klicken) |