Frage 4 - Antwort D
zurück zur Frage |
 |
Isotope haben bei gleicher Zahl von Protonen eine unterschiedliche Anzahl von Neutronen und stehen damit immer an der gleichen Stelle im Periodensystem.
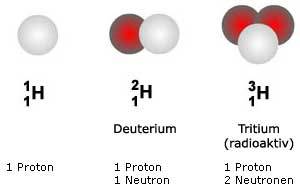
Die Atomkerne der natürlich vorkommenden
|
Beispiel: Wasserstoff Obwohl Protonium, Deuterium und Tritium über unterschiedliche Neutronenzahlen verfügen, handelt es sich chemisch jeweils um Wasserstoff. Von vielen Elementen existieren mehrere stabile Isotope (z.B. 35Cl, 37Cl für Chlor). Das führt in Abhängigkeit vom natürlichen Mischungsverhältnis der Isotope in vielen Fällen zu gebrochenen Zahlen für die Atommassen, z.B. 35,45 für Chlor (Isotopenzusammensetzung: 35Cl: ca. 75%; 35Cl: ca. 25%). Isotopengemische müssen also nicht radioaktiv sein. |
